Дегенеративные изменения кожи лица
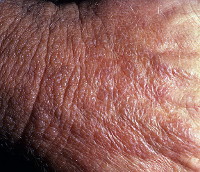
Дистрофия кожи – результат патологического течения обменных процессов в дерме, выражающийся в изменении количественного и качественного состава слоёв кожи и её дегенерации. Клинические проявления зависят от разновидности дистрофии кожи, но всегда сопровождаются истончением кожного покрова с высыпанием разнообразных первичных элементов, появлением складок кожи, меняющих её внешний вид. Диагностируют дистрофию кожи на основании типичной клиники с учётом данных гистологии. Лечение симптоматическое. Если дистрофия является симптомом какого-то заболевания, в первую очередь, необходимо диагностировать и купировать этот патологический процесс, тогда кожные проявления могут саморазрешиться.
Общие сведения
Дистрофия кожи – гетерогенные изменения в эпидермисе, дерме и подкожно-жировой клетчатке, приводящие к трансформации составляющих слои кожи элементов: коллагеновых и эластических волокон, межклеточного вещества дермы, клеток эпидермиса. Данные о распространённости, гендерной окраске, возрастных различиях, эндемичности отсутствуют, поскольку каждый из нас встречается с дистрофией кожи в качестве физиологической составляющей старения. Первые упоминания о дистрофии есть в теории порчи соков Гиппократа. В 1571 году Мальпиги, разбив кожу на слои, обосновал физиологическое старение дермы, а в конце XVIII века венский врач Пленк описал морфологию дистрофии кожи. Англичанин Г. Бейтман в 1800 году выпустил первый атлас с иллюстрациями патологии. Врождённая дистрофия кожи стала изучаться вместе с развитием генетики. Актуальность проблемы сегодня связывают с развитием онкологических процессов при некоторых формах дистрофии.

Дистрофия кожи
Причины дистрофии кожи
По своей сути, дистрофия кожи – это расстройство её трофики, врождённое или приобретённое, то есть нарушение тканевого и клеточного гомеостаза. Триггеры, запускающие процесс, разнообразны: инфекции, гипоксия, нарушение кровоснабжения тканей, энзимные инверсии, наследственность. В результате одной из причин происходит разбалансировка, как внутренней регуляции клетки, так и систем, обеспечивающих трофику кожи. В клетке возникает энергетический дефицит, ферменты перестают работать в полную силу, что является пусковым механизмом в патогенезе развития дистрофии.
«Поломки» в транспортных системах трофики (кровеносной и лимфатической) вызывают гипоксию тканей с развитием дегенеративных процессов. Параллельно возникают проблемы нейроэндокринного характера, усугубляющие трофический дисбаланс и стимулирующие развитие дегенерации. Одновременно присоединяются обменные сбои на уровне гистохимии (жировая и белковая инфильтрация тканей, синтез аномальных веществ типа амилоида), что также ускоряет дистрофию кожи. Главная опасность состоит в том, что, достигнув пика своего развития, без соответствующей корректировки процесс дегенерации становится необратимым. Физиологической иллюстрацией этого служит старение кожи.
Классификация дистрофии кожи
В современной дерматологии не существует единой классификации дистрофии кожи. В зависимости от морфологии предлагают различать паренхиматозные, мезенхимальные, смешанные дегенерации. Если взять за основу тип обменных расстройств, то можно разделить все дистрофии на белковые, жировые, минеральные, углеводные. По распространённости процесса выделяют системные и локальные дистрофии. На наш взгляд, наиболее уместно первоначальное деление дистрофии на две большие группы:
- Приобретённые дистрофии, среди которых выделяют самостоятельные заболевания (старческая дистрофия кожи, кожа земледельцев и моряков, ромбовидная гипертрофическая кожа шеи, диффузная эластома Дюбрeя, гиалома, эластоидоз кожи узелковый, дистрофия кожи пигментно-сосочковая – чёрный акантоз), и симптомы других болезней (белковая, гиалиновая, амилоидная, гидротопическая, роговая, жировая, углеводная, минеральная дистрофии).
- Врождённые дегенерационные изменения кожи представлены двумя заболеваниями: гиперэластической дистрофией Унны – наследственным аномальным гиперрастяжением дермы в результате изменений свойств коллагена и вялой дистрофией Кетли (дистрофия Алибера) – наследственной деструкцией соединительной ткани.
Симптомы дистрофии кожи
Клинически дистрофия кожи характеризуется многообразием проявлений в соответствии с разновидностями патологии. Однако есть и общие черты, присущие дистрофии. В основе своей патологический процесс дегенерации кожи представляет инволюционные преобразования клеток, как самостоятельных структурных единиц кожи, соединительной ткани и подкожно-жировой клетчатки, которые теряют своё нормальное количественное соотношение. Прежде всего, изменяется количество и структура коллагеновых, эластических волокон, эпидермальных клеток. Внешне это проявляется истончением эпидермиса, потерей тургора кожи, высыпанием множества уртикарных элементов, папул, узелков, узлов, везикул, пустул, бородавчатых образований, кератом, кист по всей поверхности кожного покрова.
Появляется ограниченная гиперпигментация кожи, она становится сухой, приобретает сероватый оттенок. Из-за потери эластичности усиливается складчатость кожи, причём начинаются такие изменения в крупных складках, на шее, в области естественных отверстий, на коленных и локтевых сгибах. В основе – дисбаланс обменных и нейрорегуляторных механизмов.
Клинические разновидности дистрофии встречаются чрезвычайно редко. Однако среди них есть один вид кожной дегенерации – чёрный акантоз, заслуживающий особого внимания. Он не имеет возрастных особенностей, но тесно связан с нарушением эндокринной сферы. Кроме того, чёрный акантоз способен малигнизироваться или долгое время существовать на фоне латентно развивающихся злокачественных новообразований других органов. Отличительной особенностью акантоза является его интенсивный серо-чёрный цвет. Первичные элементы – папилломы – плотные, грубые на ощупь, могут высыпать и на коже, и на слизистых. Интересно, что если удалить первичную опухоль, чёрный акантоз разрешается самостоятельно. Чаще других встречаются два варианта развития заболевания: ложный тип – акантоз тучных женщин с эндокринной патологией (дисфункцией яичников) и лекарственный тип, развивающийся при передозировке кортикостероидов и других лекарственных препаратов.
Диагностика и лечение дистрофии кожи
Диагностируют любую форму дегенерации кожи клинически, опираясь в сложных случаях на результаты гистологии. Дифференцируют различные разновидности дистрофии кожи между собой, а также с аддисоновой болезнью, фолликулярным дискератозом Дарье, мышьяковой меланодермией, ихтиозом, кератозом.
Лечение дистрофии симптоматическое. Обязательны консультации эндокринолога, онколога, дерматолога. При выявлении соматической патологии показано радикальное лечение с последующим диспансерным наблюдением за пациентом (онкологический контроль дважды в год). При доброкачественной дистрофии назначается витаминотерапия (А, Е, РР, D), соляные ванны, осветляющие и смягчающие кожу кремы. Отдельные папилломы небольших размеров удаляют электрокоагуляцией или лазером после консультации с косметологом. В случае массивных бородавчатых разрастаний применяют цитостатитки. Пациентам рекомендовано соблюдение оздоровительно-охранительного режима, ограниченное пребывание на солнце, дозированная физическая нагрузка, белково-витаминная диета.
Источник
К 2025 г. прогнозируемая продолжительность жизни в развитых странах достигнет 100 лет. Это приведет к увеличению численности пожилого населения, а значит, и частоты ассоциированных со старением заболеваний, в том числе кожных.
В возрасте 50+ в результате структурных изменений кожи начинает развиваться дисфункция эпидермиса, которая выражается в снижении гидратации рогового слоя, нарушении проницаемости барьера, повышении поверхностного рН. На этом фоне увеличивается риск развития или обостряются различные кожные патологии, в том числе атопический дерматит, контактный дерматит, зуд, ксероз.
В обзоре, выполненном группой специалистов под руководством Питера Элиаса, одного из начальников корнеотерапии, обсуждаются возрастные изменения эпидермиса, их связь с разными заболеваниями и способы профилактики и коррекции. Приводим часть перевода этого обзора.
Функции эпидермиса, меняющиеся с возрастом
На рисунке представлены все основные изменения эпидермиса, наблюдающиеся с возрастом. Остановимся на каждом из них подробнее.
Изменение барьерной функции
Оценка барьерной функции рогового слоя проводится путем измерения трансэпидермальной потери воды (ТЭПВ) – при нарушении барьера данный показатель резко возрастает.
У неповрежденной кожи средние нормальные значения ТЭПВ варьируют в зависимости от пола, участка тела, пигментации кожи. Что касается корреляции ТЭПВ с возрастом, то информации на эту тему не так много, и она в определенной степени противоречива. Так, в ряде работ говорится о том, что средние уровни ТЭПВ на некоторых участках тела у пожилых людей могут быть ниже, чем у молодых [1, 2], что на первый взгляд свидетельствует о более надежном барьере возрастной кожи. Вместе с тем в области декольте наблюдается возрастное увеличение ТЭПВ, что говорит об обратном [3]. На шее, предплечьях и кистях рук уровни ТЭПВ сопоставимы у молодых и пожилых женщин [3]. Также было установлено, что параметр ТЭПВ в среднем выше у пожилых женщин, чем у пожилых мужчин [4].
Несмотря на разбор результатов, ясно одно – уровни ТЭПВ в здоровой неповрежденной коже людей разного возраста хоть и несколько отличаются, но не настолько критично, чтобы говорить о патологическом нарушении барьерной функции при старении кожи. Однако возрастная проблема все же существует – после повреждения рогового слоя восстановление барьерной функции у пожилых людей происходит значительно медленнее по сравнению с более молодыми людьми. Этому есть объяснение, и оно заключается в биохимических и структурных изменениях в эпидермисе, которые проявляются с возрастом.
Напомним, что барьер проницаемости кожи локализован в роговом слое. Он состоит из корнеоцитов, заполненных кератином и окруженных белковым роговым конвертом, и чередующихся липидных и водных пластов, расположенных между корнеоцитами и регулирующих диффузию низкомолекулярных веществ через роговой слой. Функционирование барьера в значительной степени определяется количеством и качеством белковых и липидных компонентов, которые формируются в ходе созревания кератиноцитов и их финального превращения в корнеоциты.
Эпидермальный фактор роста. В эпидермисе стареющей кожи уровень эпидермального фактора роста снижается вместе с замедлением скорости деления базальных кератиноцитов. В то же время увеличивается число апоптозов кератиноцитов. Все эти приводит к истончению как живых слоев эпидермиса, так и рогового слоя [5, 6].
Ионы кальция. С возрастом наблюдается изменение градиента концентрации ионов кальция в эпидермисе – еще одного важного фактора, контролирующего деление и созревание кератиноцитов и формирование рогового слоя. Так, в базальном и шиповатом слоях эпидермиса пожилых людей концентрация кальция более высокая, что тормозит пролиферацию кератиноцитов [7, 8]. В гранулярном слое, напротив, уровень кальция падает, и это ухудшает созревание белков рогового слоя (филаггрин, лорикрин и др.) [9-11], что может привести к формированию дефектных корнеоцитов и изменению барьера проницаемости.
Межклеточные липидные пласты рогового слоя (липидный барьер). Что касается межклеточных липидных пластов, являющихся основой липидного барьера рогового слоя, то в них также выявляются возрастные изменения. Для формирования липидного барьера требуются холестерин, свободные жирные кислоты и церамиды примерно в равном молярном соотношении [12]. Эти липиды синтезируются кератиноцитами, и дефицит любого из них может привести к дефектам в барьерных структурах [13]. Исследования показали, что в «старом» роговом слое наблюдается снижение общего содержания липидов более чем на 30% по сравнению с «молодым» [2], что связано с ослаблением синтетической активности кератиноцитов – как в интактном состоянии, так и после острого повреждения. Аппликация смеси барьерных липидов может улучшить функцию барьера у пожилых людей, и это обстоятельство, в свою очередь, подтверждает наличие возрастной барьерной дисфункции [14].
рН рогового слоя. Одним из этапов формирования липидного барьера является ферментативное превращение предшественников липидов в барьерные липиды, и это превращение осуществляется уже вне кератиноцитов во внеклеточных пространствах рогового слоя [15]. Кроме ферментов, ответственных за липидный барьер, в роговом слое есть ферменты, обеспечивающие своевременное отшелушивание роговых чешуек путем разрушения корнеодесмосом (протеолитические ферменты). Все ферменты рогового слоя, как и любые другие ферменты, очень чувствительны к рН своего микроокружения. В роговом слое существует градиент рН – с кислого значения порядка 5,5 (гидролипидная мантия на поверхности кожи) к слабощелочному около 7,2 (на границе с гранулярным слоем). Таким образом, на разной глубине рогового слоя будет свой уровень рН, контролирующий работу ферментов на данной глубине (см. Вставку 1. – Прим. ред.).
С возрастом наблюдается тенденция к повышению поверхностного рН [16-17], что меняет градиент рН через роговой слой, и это сказывается на активности ферментов – протеолитические ферменты в середине и на поверхности рогового слоя при повышении рН активируются, что ускоряет отшелушивание. Напротив, ферменты, отвечающие за липидный барьер, при повышении рН угнетаются, что приводит к формированию измененного липидного барьера. Все это в совокупности приводит к ослаблению барьера проницаемости рогового слоя (см. Вставки 2 и 3. – Прим. ред.).
Аппликация препаратов с нейтральным рН задерживает восстановление барьера, напротив, подкисление рогового слоя ускоряет восстановление барьера как в молодой, так и в возрастной коже [18-20].
Глюкокортикоиды и кортизол. Биологическое старение сопровождается увеличением секреции глюкокортикоидов и повышением уровня кортизола в коже [5, 21]. Исследования показали, что системное или местное применение глюкокортикоидов тормозит пролиферацию кератиноцитов и ослабляет барьер [22]. В коже под действием 11β-гидроксистероиддегидрогеназы 1 кортизон превращается в активную форму – кортизол [23]. В возрастной коже активность этого фермента выше по сравнению с молодой [24], и это отрицательно сказывается на способности эпидермиса к восстановлению и формированию барьера [25]. Ингибирование 11β-гидроксистероиддегидрогеназы 1 не только корректирует вызванные глюкокортикоидами эпидермальные функциональные нарушения, но и способствует восстановлению структуры барьера [26, 27].
Другие факторы. Есть и другие факторы, связанные со старением изменения кожи, которые могут способствовать изменению функции эпидермиса. Например, по сравнению с молодым эпидермисом в стареющем эпидермисе наблюдается более чем 60% снижение уровня белка-антагониста рецептора ИЛ-1, а дефицит рецептора ИЛ-1α типа 1 задерживает восстановление барьера [28]. Напротив, как повышение экспрессии, так и введение ИЛ-1α укрепляет барьер как в стареющей коже, так и в коже плода [29, 30].
В стареющей коже также наблюдается снижение количества гиалуроновой кислоты. Исследования показали: местное применение гиалуроновой кислоты стимулирует дифференцировку кератиноцитов и выработку липидов, что приводит к усилению функции эпидермального барьера проницаемости как в молодой, так и в пожилой коже [31, 32].
Наконец, с возрастом наблюдается снижение экспрессии эпидермального аквапорина-3 – белка, формирующего водные каналы в мембране кератиноцитов и отвечающего за внутриклеточный водный баланс [32-34]. Выключение гена, кодирующего аквапорин-3, задерживает восстановление барьера проницаемости [35]. Напротив, усиление экспрессии аквапорина-3 улучшает барьерную функцию [36].
Снижение гидратации рогового слоя
Примерно после 40 лет уровень гидратации рогового слоя начинает снижаться. Механизмы, лежащие в основе уменьшения гидратации рогового слоя в стареющей коже, можно объяснить дефицитом веществ, входящих в водорегулирующие и водоудерживающие его структуры.
Во-первых, в роговом слое стареющей кожи снижается количество барьерных липидов [2, 37], в том числе церамидов [38]. Их дефицит можно компенсировать путем перорального или местного применения церамидов, что приводит к повышению гидратации рогового слоя [39, 40].
Во-вторых, снижается уровень филаггрина [11] и его метаболитов, включая транс-урокановую и пироглутаминовую кислоты, входящие в состав натурального увлажняющего фактора (NMF). Аппликации этих веществ, а также и других компонентов NMF, таких как свободные аминокислоты, молочная кислота и мочевина, способствуют повышению гидратации рогового слоя.
В-третьих, в возрастной коже по сравнению с молодой ниже продукция себума в целом и глицерина в частности [16, 41]. Себум вместе с секретом потовых желез формирует гидролипидную мантию, регулирующую испарение воды с поверхности кожи. Если мантия нарушена, испарение усиливается, поэтому в себодефицитной коже наблюдается снижение гидратации рогового слоя, и аппликация препаратов, имитирующих гидролипидную мантию, помогает ее восстановить.
Наконец, в возрастном эпидермисе снижается уровень аквапорина-3 [33-35]. Это ухудшает движение воды в живых слоях эпидермиса и способствует развитию застойных явлений, на фоне которых тормозится деление и созревание кератиноцитов. Аквапориновые каналы могут активироваться в присутствии небольшого количества глицерина (несколько процентов) в окружающей среде [42], высокие концентрации глицерина (свыше 10%), напротив, ингибируют их работу.
Повышение pH поверхности кожи
Значение pH поверхности кожи человека в первые две недели жизни обычно выше, к 5-6-й нед оно снижается до среднего 5,5 [43]. После 55 лет pH поверхности кожи имеет тенденцию к повышению, и у людей старше 70 это повышение становится существенным [16, 18]. Нормальные значения pH поверхности кожи человека зависят от пола и участка тела [44].
Возрастное повышение рН поверхности кожи связано с несколькими факторами. Один из них – уменьшение продукции себума и, соответственно, количества триглицеридов [3, 16], из которых высвобождаются свободные жирные кислоты, подкисляющие гидролипидную мантию и поверхность рогового слоя [45]. В нижних слоях роговой слой подкисляется благодаря высвобождению свободных жирных кислот из фосфолипидов клеточных мембран под действием секреторной фосфолипазы 2 (sPLA2) [46], экспрессия которой заметно снижается с возрастом.
Натрий-водородный обменник 1 (NHE1) – еще один механизм, регулирующий градиент pH в роговом слое: при дефиците NHE1 pH поверхности кожи повышается [47]. В стареющей коже экспрессия NHE1 значительно ниже, чем в молодой коже, что может способствовать повышению поверхностного рН.
И наконец, в стареющей коже наблюдается низкий уровень экспрессии филаггрина [10], который может расщепляться до транс-урокановой кислоты по филаггрин-гистидин-урокановокислотному пути [48]. Урокановая кислота подкисляет роговой слой [49].
Узнать больше о последствиях возрастных изменений эпидермиса, а также подходах к улучшению эпидермальных функций в стареющей коже – что именно нужно делать, чтобы поддержать здоровье кожи, вы можете в полной версии статьи, опубликованной у журнале «Косметика и медицина» №4-2020. Журнал доступен в печатной и электронной версии. Рекомендуем – там еще много очень интересных материалов!
Литература:
© Wang Z., Man M.Q., Tienan L., et al. Aging-associated alterations in epidermal and their clinical ificance. Aging 2020; 12(6): 5551-5565. Перевод и публикация в сокращенном виде – в соответствии с лицензией Creative Commons Attribution License.
- Boireau-Adamezyk E., Baillet-Guffroy A., Stamatas G.N. Age-dependent changes in stratum corneum barrier . Skin Res Technol 2014; 20(4): 409-415.
- Ghadially R., Brown B.E., Sequeira-Martin S.M., et al. The aged epidermal permeability barrier. Structural, al, and lipid biochemical abnormalities in humans and a senescent murine model. J Clin Invest 1995; 95(5): 2281-2290.
- Luebberding S., Krueger N., Kerscher M. Age- changes in skin barrier – quantitative evaluation of 150 female subjects. Int J Cosmet Sci 2013a; 35(2): 183-190.
- Luebberding S., Krueger N., Kerscher M. Skin physiology in men and women: in vivo evaluation of 300 people including TEWL, SC hydration, sebum content and skin surface pH. Int J Cosmet Sci 2013b; 35(5): 477-483.
- Kinn P.M., Holdren G.O., Westermeyer B.A., et al. Age-dependent variation in cytokines, chemokines, and biologic analytes rinsed from the surface of healthy human skin. Sci Rep 2015; 5: 10472.
- Gilhar A., Ullmann Y., Karry R., et al. Aging of human epidermis: reversal of aging changes correlates with reversal of keratinocyte fas expression and apoptosis. J Gerontol A Biol Sci Med Sci 2004; 59(5): 411-415.
- Micallef L., Belaubre F., Pinon A., et al. Effects of cellular calcium on the growth-differentiation switch in immortalized keratinocyte HaCaT cells compared with normal human keratinocytes. Exp Dermatol 2009; 18(2): 143-151.
- Denda M., Tomitaka A., Akamatsu H., Matsunaga K. Altered distribution of calcium in facial epidermis of aged adults. J Invest Dermatol 2003; 121(6): 1557-1558.
- Tezuka T., Qing J., Saheki M., et al. Terminal differentiation of facial epidermis of the aged: immunohistochemical studies. Dermatology 1994; 188(1): 21-24.
- Rinnerthaler M., Duschl J., Steinbacher P., et al. Age- changes in the composition of the cornified envelope in human skin. Exp Dermatol 2013; 22(5): 329-335.
- Takahashi M., Tezuka T. The content of free amino acids in the stratum corneum is increased in senile xerosis. Arch Dermatol Res 2004; 295(10): 448-452.
- Man M.Q., Feingold K.R., Thornfeldt C.R., Elias P.M. Optimization of physiological lipid mixtures for barrier repair. J Invest Dermatol. 1996; 106(5): 1096-1101.
- Feingold K.R., Elias P.M. Role of lipids in the formation and maintenance of the cutaneous permeability barrier. Biochim Biophys Acta 2014; 1841(3): 280-294.
- Zettersten E.M., Ghadially R., Feingold K.R., et al. Optimal ratios of topical stratum corneum lipids improve barrier recovery in chronologically aged skin. J Am Acad Dermatol 1997; 37(3 Pt 1): 403-408.
- Man M.Q., Feingold K.R., Jain M., Elias P.M. cellular processing of phospholipids is required for permeability barrier homeostasis. J Lipid Res 1995; 36(9): 1925-1935.
- Man M.Q., Xin S.J., Song S.P., et al. Variation of skin surface pH, sebum content and stratum corneum hydration with age and gender in a large Chinese population. Skin Pharmacol Physiol 2009; 22(4): 190-199.
- Schreml S., Zeller V., Meier R.J., et al. Impact of age and body site on adult female skin surface pH. Dermatology 2012; 224(1): 66-71.
- Choi E.H., Man M.Q., Xu P., et al. Stratum corneum acidification is impaired in moderately aged human and murine skin. J Invest Dermatol 2007; 127(12): 2847-2856.
- Hachem J.P., Roelandt T., Schürer N., et al. Acute acidification of stratum corneum membrane domains using polyhydroxyl acids improves lipid processing and inhibits degradation of corneodesmosomes. J Invest Dermatol 2010; 130(2): 500-510.
- Hachem J.P., Crumrine D., Fluhr J., et al. pH directly regulates epidermal permeability barrier homeostasis, and stratum corneum integrity/cohesion. J Invest Dermatol 2003; 121(2): 345-353.
- Yiallouris A., Tsioutis C., Agapidaki E., et al. Adrenal Aging and Its Implications on Stress Responsiveness in Humans. Front Endocrinol (Lausanne) 2019; 10: 54.
- Kao J.S., Fluhr J.W., Man M.Q., et al. Short-term glucocorticoid treatment compromises both permeability barrier homeostasis and stratum corneum integrity: inhibition of epidermal lipid synthesis accounts for al abnormalities. J Invest Dermatol 2003; 120(3): 456-464.
- Tomlinson J.W., Walker E.A., Bujalska I.J., et al. 11beta-hydroxysteroid dehydrogenase type 1: a tissue-specific regulator of glucocorticoid response. Endocr Rev 2004; 25(5): 831-866.
- Tiganescu A., Walker E.A., Hardy R.S., et al. Localization, age- and site-dependent expression, and regulation of 11β-hydroxysteroid dehydrogenase type 1 in skin. J Invest Dermatol 2011; 131(1): 30-36.
- Choe S.J., Kim D., Kim E.J., et al. Psychological Stress Deteriorates Skin Barrier by Activating 11β-Hydroxysteroid Dehydrogenase 1 and the HPA Axis. Sci Rep 2018; 8(1): 6334.
- Tiganescu A., Hupe M., Uchida Y., et al. Topical 11β-Hydroxysteroid Dehydrogenase Type 1 Inhibition Corrects Cutaneous Features of Systemic Glucocorticoid Excess in Female Mice. Endocrinology 2018; 159(1): 547-556.
- Tiganescu A., Tahrani A.A., Morgan S.A., et al. 11β-Hydroxysteroid dehydrogenase blockade prevents age-induced skin structure and defects. J Clin Invest 2013; 123(7): 3051-3060.
- Ye J., Garg A., Calhoun C., et al. Alterations in cytokine regulation in aged epidermis: implications for permeability barrier homeostasis and inflammation. I. IL-1 gene family. Exp Dermatol 2002; 11(3): 209-216.
- Barland C.O., Zettersten E., Brown B.S., et al. Imiquimod-induced interleukin-1 alpha stimulation improves barrier homeostasis in aged murine epidermis. J Invest Dermatol 2004; 122(2): 330-336.
- Jiang Y.J., Lu B., Crumrine D., et al. IL-1alpha accelerates stratum corneum formation and improves permeability barrier homeostasis during murine fetal development. J Dermatol Sci 2009; 54(2): 88-98.
- Bourguignon L.Y., Ramez M., Gilad E., et al. Hyaluronan-CD44 interaction stimulates keratinocyte differentiation, lamellar body formation/secretion, and permeability barrier homeostasis. J Invest Dermatol 2006; 126(6): 1356-1365.
- Bourguignon L.Y., Wong G., Xia W., et al. Selective matrix (hyaluronan) interaction with CD44 and RhoGTPase aling tes keratinocyte s and overcomes age- epidermal dys. J Dermatol Sci 2013; 72(1): 32-44.
- Li J., Tang H., Hu X., et al. Aquaporin-3 gene and protein expression in sun-protected human skin decreases with skin ageing. Australas J Dermatol 2010; 51(2): 106-112.
- Ikarashi N., Kon R., Kaneko M., et al. Relationship between Aging- Skin Dryness and Aquaporins. Int J Mol Sci 2017; 18(7): E1559.
- Hara M., Ma T., Verkman A.S. Selectively reduced glycerol in skin of aquaporin-3-deficient mice may account for impaired skin hydration, elasticity, and barrier recovery. J Biol Chem 2002; 277(48): 46616-46621.
- Schrader A., Siefken W., Kueper T., et al. Effects of glyceryl glucoside on AQP3 expression, barrier and hydration of human skin. Skin Pharmacol Physiol 2012; 25(4): 192-199.
- Rogers J., Harding C., Mayo A., et al. Stratum corneum lipids: the effect of ageing and the seasons. Arch Dermatol Res 1996; 288(12): 765-770.
- Imokawa G., Abe A., Jin K., et al. Decreased level of ceramides in stratum corneum of atopic dermatitis: an etiologic factor in atopic dry skin? J Invest Dermatol 1991; 96(4): 523-526.
- Bizot V., Cestone E., Michelotti A., Nobile V. Improving Skin Hydration and Age- Symptoms by Oral Administration of Wheat Glucosylceramides and Digalactosyl Diglycerides: A Human Clinical Study. Cosmetics 2017; 4(4): 37.
- Huang H.C., Chang T.M. Ceramide 1 and ceramide 3 act synergistically on skin hydration and the transepidermal water loss of sodium lauryl sulfate-irritated skin. Int J Dermatol 2008; 47(8): 812-819.
- Choi E.H., Man M.Q., Wang F., et al. Is endogenous glycerol a determinant of stratum corneum hydration in humans? J Invest Dermatol 2005; 125(2): 288-293.
- Dumas M., Sadick N.S., Noblesse E., et al. Hydrating skin by stimulating biosynthesis of aquaporins. J Drugs Dermatol 2007; 6(6 Suppl): s20-s24.
- Fluhr J.W., Darlenski R., Lachmann N., et al. Infant epidermal skin physiology: adaptation after birth. Br J Dermatol 2012; 166(3): 483-490.
- Zlotogorski A. Distribution of skin surface pH on the fore and cheek of adults. Arch Dermatol Res 1987; 279(6): 398-401.
- Yamamoto A., Serizawa S., Ito M., Sato Y. Effect of aging on sebaceous gland activity and on the fatty acid composition of wax esters. J Invest Dermatol 1987; 89(5): 507-512.
- Fluhr J.W., Kao J., Jain M., et al. Generation of free fatty acids from phospholipids regulates stratum corneum acidification and integrity. J Invest Dermatol 2001; 117(1): 44-51.
- Behne M.J., Meyer J.W., Hanson K.M., et al. NHE1 regulates the stratum corneum permeability barrier homeostasis. Microenvironment acidification assessed with fluorescence life imaging. J Biol Chem 2002; 277(49): 47399-47406.
- Vávrová K., Henkes D., Strüver K., et al. Filaggrin deficiency leads to impaired lipid profile and altered acidification pathways in a 3D skin construct. J Invest Dermatol 2014; 134(3): 746-753.
- Krien P.M., Kermici M. Evidence for the existence of a self-regulated enzymatic process within the human stratum corneum -an unexpected role for urocanic acid. J Invest Dermatol 2000; 115(3): 414-420.
Источник
